新药研究对国家的经济发展、社会进步和国家安全具有重大而深远的影响。药物是人类与疾病斗争的重要武器,对于保障人民生命和健康起着关键作用。现代医药产业又是一项迅速发展的高新技术产业,是新世纪的经济增长点和重要支柱产业。创新药物的研究与开发,是基础研究和应用研究紧密结合的科技创新活动,是推动科技发展和进步的强大动力,也是生命科学和生物技术科技成果产业化的重要途径。因此,创新药物的研发已经成为新世纪科技和经济国际竞争的战略制高点之一,各国政府、研发机构和制药公司均高度重视创新药物研发,我国《国家中长期科学和技术发展规划纲要(2006-2020年)》已明确“靶标发现技术”和“药物分子设计技术”为今后重点发展的前沿技术。
目前的计算药物设计和技术是基于分子与靶标的结合亲和性越强,化合物的活性可能越高这种假设发展的。但对临床用药的统计结果表明,药物的体内药效与结合亲和性没有直接的相关性,而与药物-靶标结合的动力学(Kinetics)参数,特别是药物-靶标驻留时间(Residence Time)τ(τ=1/ koff, koff为解离速率常数)直接相关[1-3]。药物-靶标结合是一个动态过程,结合亲和力是药物-靶标相互作用达到平衡时的热力学性质;另一方面,药物与靶标结合和解离的动力学性质主要由结合速率常数(kon)解离速率常数(koff)决定。理论上,解离速率常数越小,药物在靶标活性部位“逗留”的时间越长,药效越好。此外,药物-靶标结合驻留时间还与药物的选择性和毒副作用有关,药物与药效相关靶标结合的驻留时间长,而与药效无关或毒副作用相关靶标不结合或结合的驻留时间短,则药物的选择性就好,毒性就低[4, 5]。
药物与靶标相互作用(结合)的动力学过程可以用化学反应动力学理论来描述:即,可以把药物(D)和靶标(R)当作反应物(Reactant),把药物和靶标结合后形成的复合物当作产物(Product),把药物和靶标结合形成复合物的过程当作一个可逆反应,正反应速率常数为kon,逆反应速率常数为koff。由化学反应过渡态理论可知,药物和靶标结合形成复合物过程中需经过一个或几个过渡态[6, 7],即翻越一个或多个能垒;同样,药物从结合靶标上解离时也需翻越一个或多个能垒。这些能垒用活化能( )或活化自由能(
)或活化自由能( )表示。
)表示。
结合自由能与结合速率常数的关系如下:
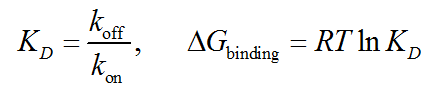
(1)
药物-靶标结合或解离活化自由能与反应速率常数间的关系由Ering-Polanyi方程[8,9]给出:
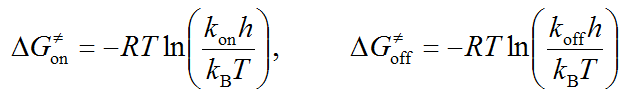
(2)
其中,h是普朗克(Planck)常数,kB是玻尔兹曼(Boltzmann)常数,T是绝对温度。药物-靶标结合自由能与活化自由能的关系为:
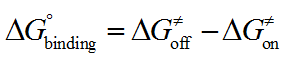
(3)
另一个非常重要的药物-靶标结合动力学参数是,药物与靶标结合后在靶标结合部位(口袋)的驻留时间τ[3,10]。驻留时间是药物-靶标解离速率常数的倒数,即:
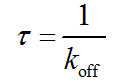
(4)
通常采用解离半衰期τ1/2表征药物-靶标相互作用的动力学行为:
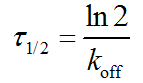
(5)
因此,在药物设计中,通过考虑提高药物与目标靶标的结合保留时间,并降低药物与其他无关或毒性相关靶标的结合保留时间,是发现高效低毒药物的一个可行途径[11-13]。
参考文献:
1. Zhang, R., and Monsma, F. (2010). Binding kinetics and mechanism of action: toward the discovery and development of better and best in class drugs. Expert Opinion on Drug Discovery 5, 1023-1029.
2. Swinney, D.C. (2009). The role of binding kinetics in therapeutically useful drug action. Curr Opin Drug Discov Devel 12, 31-39.
3. Copeland, R.A., Pompliano, D.L., and Meek, T.D. (2006). Drug-target residence time and its implications for lead optimization. Nat Rev Drug Discov 5, 730-739.
4.Copeland R. A. Conformational adaptation in drug-target interactions and residence time . Future Medicinal Chemistry, 2011, 3(12):1491-1501.
5.Yan Z., Zheng X., Wang E., et al. Thermodynamic and kinetic specificities of ligand binding. Chemical Science, 2013, 4(6):2387-2395.
6.Laidler K. J., King M. C. Development of transition-state theory. The Journal of Physical Chemistry, 1983, 87(15):2657-2664.
7.Pechukas P. Transition State Theory. Annual Review of Physical Chemistry, 1981, 32(1):159-177.
8.Winzor D. J., Jackson C. M. Interpretation of the temperature dependence of equilibrium and rate constants. Journal of Molecular Recognition, 2006, 19(5):389-407.
9.Evans M. G., Polanyi M. Some applications of the transition state method to the calculation of reaction velocities, especially in solution. Transactions of the Faraday Society, 1935, 31(0):875-894.
10.Copeland R. A. The dynamics of drug-target interactions: drug-target residence time and its impact on efficacy and safety. Expert Opinion on Drug Discovery, 2010, 5(4):305-310.
11.郭颖,郭宗儒. 药物与受体靶标结合动力学对体内药效的影响. 中国药物化学杂志, 2014, 24(1):70-77.
12.郭颖,郭宗儒.从噻托溴铵谈药物与受体的结合动力学. 中国新药杂志, 2013, 22(20):2353-2357.
13. Bai, F., Xu, Y., Chen, J., Liu, Q., Gu, J., Wang, X., Ma, J., Li, H., Onuchic, J.N., Jiang, H.Free energy landscape for the binding process of Huperzine A to acetylcholinesterase.Proc Natl Acad Sci U S A. 2013, 110(11):4273-4278.